Đề kiểm tra 1 tiết (bài số 4) - Môn: Hóa Học 10 - Mã đề: 143
Câu 1 : Cho 44,5 gam hỗn hợp bột Zn và Mg tác dụng với dung dịch HCl dư thấy có 22,4 lit khí H2 bay ra (đktc). Khối lượng muối clorua tạo ra trong dung dịch là:
A. 80 gam B. 115,5 gam C. 97,75 gam D. 90 gam
Câu 2 : Khi nung nóng, iot biến thành hơi không qua trạng thái lỏng. Hiện tượng này được gọi là:
A. Sự chuyển trạng thái B. Sự thăng hoa C. Sự phân hủy D. Sự bay hơi
Câu 3 : Chất nào sau đây thường được dùng để diệt khuẩn và tẩy màu?
A. O2 B. Cl2 C. N2 D. CO2
Câu 4 : Kim loại nào khi tác dụng với clo và axit clohidric cho cùng một loại muối?
A. Ag B. Zn C. Fe D. Cu
Câu 5 : Rót dung dịch AgNO3 vào 4 lọ dd riêng biệt: NaF, NaCl, NaBr, NaI. Có mấy lọ tạo kết tủa?
A. 3 B. 1 C. 2 D. 4
Câu 6 : Trong dãy các axit halogenhiđric, axit nào mạnh nhất?
A. HCl B. HBr C. HI D. HF
Câu 7 : Dãy chất nào sau đây đều tác dụng với dd HCl:
A. Cu, Al, NaOH B. Na, Br2, H2SO4 C. Mg, FeO, Ba(OH)2 D. Quỳ tím, Ag, AgNO3
Câu 8 : Thuốc thử để nhận biết ion clorua là:
A. dd Na2CO3 B. dd NaOH C. dd AgNO3 D. Quỳ tím
Câu 9 : Cho hỗn hợp 2 muối MgCO3 và CaCO3 tan trong dung dịch HCl vừa đủ tạo ra 2,24 lít khí (đktc). Số mol của 2 muối cacbonat ban đầu là:
A. 0,15 mol B. 0,2 mol C. 0,1 mol D. 0,3 mol
Câu 10 : Khi mở vòi nước máy, nếu chú ý một chút sẽ phát hiện mùi lạ. Đó là do nước máy còn lưu giữ vết tích của thuốc sát trùng chính là clo và người ta giải thích khả năng diệt khuẩn là do:
A. Clo độc nên có tính sát trùng.
B. Clo tác dụng với nước tạo ra kháng thể diệt khuẩn.
C. Clo có thể phát ra tia cực tím.
D. Clo tác dụng với nước tạo ra HClO chất này có tính oxi hóa mạnh.
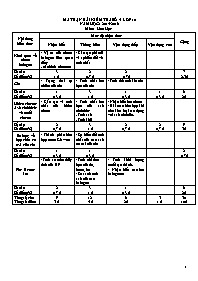
MA TRẬN BÀI KIỂM TRA SỐ 4 LỚP 10 NĂM HỌC: 2015-2016 Môn: Hóa Học Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng thấp Vận dụng cao Khái quát về nhóm halogen - Vị trí của nhóm halogen liên quan đến: . cấu hình electron - Cấu tạo phân tử và sự biến đổi về tính chất Số câu Số điểm(%) 3 1 đ 2 0.7 đ 2 0,7đ 7 2,3đ Clo - Trạng thái tự nhiên của clo - Tính chất hóa học của clo - Tính thể tích khí clo Số câu Số điểm(%) 1 0,3 đ 3 1 đ 1 0,3 đ 1 0,3 đ 6 2đ Hiđro clorua- Axit clohiđric và muối clorua - Cấu tạo và tính chất của hiđro clorua - Tính chất hóa học của axit clohđric: . Tính axit . Tính khử - Nhận biết ion clorua - Bài toán hỗn hợp khi cho kim loại tác dụng với axit clohđic. Số câu Số điểm(%) 2 0,7 đ 3 1 đ 2 0,7 đ 2 0,7 đ 9 3đ Sơ lược về hợp chất có oxi của clo - Thành phần hỗn hợp nước Gia-ven - Sự biến đổi tính chất của các axit có oxi của clo Số câu Số điểm(%) 1 0,3 đ 1 0,3 đ 2 0,7đ Flo- Brom- Iot - Tính ăn mòn thủy tinh của HF - Tính chất hóa học của flo, brom, iot - So sánh tính axit của các halogen - Tính khối lượng muối tạo thành. - Nhận biết các ion halogenua Số câu Số điểm(%) 2 0,7 đ 3 1 đ 1 0,3 đ 6 2đ Tổng số câu Tổng số điểm 9 3 đ 12 4 đ 6 2đ 3 1 đ 30 10đ SỞ GD-ĐT NINH THUẬN ĐỀ KIỂM TRA 1 TIẾT (BÀI SỐ 4) - LỚP 10 TRƯỜNG THPT BÁC ÁI NĂM HỌC 2015-2016 Môn: Hóa học – Chương trình chuẩn Mã đề: 143 Thời gian làm bài: 45 phút (Không kể thời gian phát đề) Đề ra: (Đề kiểm tra có 02 trang) Câu 1 : Cho 44,5 gam hỗn hợp bột Zn và Mg tác dụng với dung dịch HCl dư thấy có 22,4 lit khí H2 bay ra (đktc). Khối lượng muối clorua tạo ra trong dung dịch là: A. 80 gam B. 115,5 gam C. 97,75 gam D. 90 gam Câu 2 : Khi nung nóng, iot biến thành hơi không qua trạng thái lỏng. Hiện tượng này được gọi là: A. Sự chuyển trạng thái B. Sự thăng hoa C. Sự phân hủy D. Sự bay hơi Câu 3 : Chất nào sau đây thường được dùng để diệt khuẩn và tẩy màu? A. O2 B. Cl2 C. N2 D. CO2 Câu 4 : Kim loại nào khi tác dụng với clo và axit clohidric cho cùng một loại muối? A. Ag B. Zn C. Fe D. Cu Câu 5 : Rót dung dịch AgNO3 vào 4 lọ dd riêng biệt: NaF, NaCl, NaBr, NaI. Có mấy lọ tạo kết tủa? A. 3 B. 1 C. 2 D. 4 Câu 6 : Trong dãy các axit halogenhiđric, axit nào mạnh nhất? A. HCl B. HBr C. HI D. HF Câu 7 : Dãy chất nào sau đây đều tác dụng với dd HCl: A. Cu, Al, NaOH B. Na, Br2, H2SO4 C. Mg, FeO, Ba(OH)2 D. Quỳ tím, Ag, AgNO3 Câu 8 : Thuốc thử để nhận biết ion clorua là: A. dd Na2CO3 B. dd NaOH C. dd AgNO3 D. Quỳ tím Câu 9 : Cho hỗn hợp 2 muối MgCO3 và CaCO3 tan trong dung dịch HCl vừa đủ tạo ra 2,24 lít khí (đktc). Số mol của 2 muối cacbonat ban đầu là: A. 0,15 mol B. 0,2 mol C. 0,1 mol D. 0,3 mol Câu 10 : Khi mở vòi nước máy, nếu chú ý một chút sẽ phát hiện mùi lạ. Đó là do nước máy còn lưu giữ vết tích của thuốc sát trùng chính là clo và người ta giải thích khả năng diệt khuẩn là do: A. Clo độc nên có tính sát trùng. B. Clo tác dụng với nước tạo ra kháng thể diệt khuẩn. C. Clo có thể phát ra tia cực tím. D. Clo tác dụng với nước tạo ra HClO chất này có tính oxi hóa mạnh. Câu 11 : Chất nào sau đây chỉ có tính oxi hoá, không có tính khử? A. F2 B. Cl2 C. Br2 D. I2 Câu 12 : Clo không phản ứng với chất nào sau đây? A. NaOH B. Al C. NaCl D. NaBr Câu 13 : Theo chiều tăng điện tích hạt nhân thì khả năng oxi hóa của các halogen theo thứ tự: A. tăng rồi giảm B. giảm dần C. tăng dần D. không thay đổi Câu 14 : Axit clohidric có thể tham gia phản ứng oxi hóa - khử với vai trò: A. Môi trường B. Chất khử C. Chất xúc tác D. Chất oxi hóa Câu 15 : Dung dịch nào sau đây không phản ứng với dung dịch AgNO3? A. BaCl2 B. NaBr C. NaI D. HF Câu 16 : Cấu hình e lớp ngoài cùng của nguyên tử các nguyên tố halogen là: A. ns2p5 B. ns2np4 C. ns2np3 D. ns2np6 Câu 17 : Để nhận biết 4 lọ mất nhãn đựng HCl, KOH, Ca(NO3)2, BaCl2, thuốc thử cần dùng là: A. Quỳ tím B. AgNO3 C. NaOH D. Quỳ tím; AgNO3 Câu 18 : Clorua vôi gọi là muối hỗn tạp vì được tạo bởi một kim loại liên kết với: A. Ba loại gốc axit B. Nhóm hiđroxit C. Một loại gốc axit D. Hai loại gốc axit Câu 19 : X là muối thu được khi cho Fe tác dụng với khí Clo; Y là muối thu được khi cho Fe tác dụng với dd HCl. X và Y lần lượt là: A. Đều là FeCl3 B. FeCl3, FeCl2 C. Đều là FeCl2 D. FeCl2, FeCl3 Câu 20 : Để tẩy uế trong bệnh viện người ta thường dùng: A. Tia phóng xạ B. Clorua vôi C. Khí ozon D. Nước Gia–ven Câu 21 : Cho 4,6g Na tác dụng với 4,48l khí Cl 2. Khối lượng muối thu được là: A. 23,4g B. 5,85g C. 11,7g D. 14,35g Câu 22 : Phản ứng nào sau đây chứng tỏ HCl có thể là chất khử? A. HCl + NaOH → NaCl + H2O B. 2HCl + Mg → MgCl2 + H2↑ C. NH3 + HCl → NH4Cl D. MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O Câu 23 : Cho khí clo tác dụng với 0,448l khí hiđro. Thể tích khí thu được sau pư ở đktc là: A. 0,448l B. 1,12l C. 1,008l D. 0,896l Câu 24 : Số oxi hóa mà các nguyên tố Halogen đều có trong các hợp chất là: A. −1 B. +1; +3; +5; +7 C. 0 D. −1; 0; +1; +3; +5; +7 Câu 25 : Các halogen có tính chất hóa học gần giống nhau vì có cùng: A. Tính oxi hóa mạnh. B. Cấu hình e lớp ngoài cùng. C. Số e. D. Số lớp e. Câu 26 : Axit không thể đựng trong bình thủy tinh là: A. HNO3 B. H2SO4 C. HBr D. HF Câu 27 : Nhận định nào sau đây sai khi nói về flo? A. Là chất lỏng, màu nâu đỏ B. Là phi kim loại hoạt động mạnh nhất C. Là chất oxi hoá rất mạnh D. Có độ âm điện lớn nhất Câu 28 : Thuốc thử để nhận biết I2 là: A. Hồ tinh bột B. Na C. Quỳ tím D. dd AgNO3 Câu 29 : Nhận xét nào sau đây về nhóm halogen là không đúng: A. Đều tác dụng được với nước B. Tác dụng với kim loại tạo muối halogenua. C. Có đơn chất ở dạng X2 D. Tác dụng với hiđro tạo khí hiđro halogenua Câu 30 : Đặc điểm nào không phải là đặc điểm chung của các halogen? A. Đều là chất khí ở điều kiện thường. B. Đều có tính oxi hóa mạnh. C. Tác dụng với hầu hết các kim loại D. Khả năng tác dụng với nước giảm dần tử F2 đến I2. --- Hết --- SỞ GD – ĐT NINH THUẬN TRƯỜNG THPT BÁC ÁI Đề chính thức ĐỀ KIỂM TRA 1 TIẾT (BÀI SỐ 4) – LỚP 10 NĂM HỌC 2015 – 2016 Môn: Hóa học – Chương trình chuẩn Thời gian làm bài: 45 phút (Không kể thời gian phát đề) BẢNG ĐÁP ÁN ĐỀ 143 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 B B B B A C C C C D A C C B D 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 A D D B B C D D A B D A A A A
Tài liệu đính kèm:
 de_kiem_tra_1_tiet_bai_so_4_mon_hoa_hoc_10_ma_de_143.doc
de_kiem_tra_1_tiet_bai_so_4_mon_hoa_hoc_10_ma_de_143.doc





