Đề kiểm tra học kỳ II lớp 10 - Môn: Hóa
Câu 1: Kim loại nào sau đây sẽ bị thụ động khi gặp dung dịch H2SO4 đặc, nguội?
A. Al và Fe B. Al và Zn. C. Fe và Mg. D. Fe và Cu.
Câu 2: Chất nào sau đây được dùng để tẩy màu, sát trùng ?
A. N2 B. CaOCl2 C. NaOH D. KNO3
Câu 3: Cho phản ứng hóa học: Cl2 + 2NaOH NaCl + NaClO + H2O. Vai trò của Cl2 trong phản ứng này là:
A. Không là chất oxi hóa, không là chất khử B. Chất oxi hóa
C. Chất khử D. Vừa là chất oxi hóa, vừa là chất khử
Câu 4: Chất dùng để chữa sâu răng trong y học là:
A. H2S B. O2 C. O3 D. Cl2
Câu 5: Chất khí màu vàng lục, rất độc là:
A. SO2 B. Cl2 C. Br2 D. F2
Câu 6: Phản ứng được dùng để điều chế SO2 trong công nghiệp là:
A. Cu + 2H2SO4(đ) CuSO4 + SO2 + 2H2O B. 4FeS2 + 11O2 2Fe2O3 + 8SO2
C. C + 2H2SO4(đ) CO2 + 2SO2 + 2H2O D. 2H2S + 3O2 2SO2 + 2H2O
Câu 7: Nguyên tử của các nguyên tố F, Cl, Br, I đều có?
A. 6 electron ở lớp ngoài cùng B. 1 electron ở lớp ngoài cùng
C. 7 electron ở lớp ngoài cùng D. 5 electron ở lớp ngoài cùng
Câu 8: Phản ứng hóa học nào sau đây chứng tỏ Cl2 có tính oxi hóa mạnh hơn Br2?
A. Cl2 +2NaBr 2NaCl + Br2 B. Cl2 + H2O HCl + HClO
C. Cl2 + 2NaI 2NaCl + I2 D. Br2 +2NaI 2NaBr + I2
Câu 9: Phản ứng giữa 2 chất nào sau đây xảy ra dễ dàng nhất?
A. I2 và H2. B. F2 và H2. C. Br2 và H2 D. Cl2 và H2.
Câu 10: Ở điều kiện thường, O3 oxi hóa được kim loại nào sau đây mà O2 không phản ứng được?
A. Ag B. Mg C. Cu D. Fe
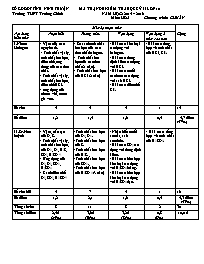
SỞ GD&ĐT TỈNH NINH THUẬN MA TRẬN ĐỀ KIỂM TRA HỌC KỲ II LỚP 10 Trường THPT Trường Chinh NĂM HỌC: 2015 – 2016 Môn: HÓA Chương trình: CHUẨN Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng Vận dụng ở mức cao hơn I. Nhóm Halogen - Vị trí của các nguyên tố. - Tính chất vật lý, tính chất hóa học, điều chế, ứng dung của các đơn chất. - Tính chất vật lý, tính chất hóa học, điều chế HCl. - ứng dụng của clorua vôi, nước gia ven. - So sánh tính chất hóa học của các đơn chất halogen. - Tính chất hóa học của các đơn chất (2 câu). - Tính chất hóa học của HCl (2 câu) - Bài toán kim loại tác dụng với halogen. - Bài toán dung dịch kiềm tác dụng với HCl. - Bài toán muối cacbonat tác dụng với axit HCl. - Bài toán điều chế Cl2. - Bài toán tổng hợp về tính chất của HCl, Cl2. Số câu 4 5 4 1 14 Số điểm 1,2 1,5 1,6 0,4 4,7 điểm (47%) II. Oxi-lưu huỳnh - Vị trí, cấu tạo của O, S. - Tính chất vật lý, tính chất hóa học, của O2, O3, H2S, SO2, H2SO4. - Ứng dụng của O2, O3, SO2, H2SO4 - Cách điều chế O2, SO2, H2SO4 -Tính chất hóa học của O2, O3. -Tính chất hóa học của S. -Tính chất hóa học của H2S. -Tính chất hóa học của SO2. -Tính chất hóa học của H2SO4 (3 câu). - Nhận biết muối sunfat, axit sunfuric. - Bài toán SO2 tác dụng với dung dịch kiềm. - Bài toán hỗn hợp kim loại tác dụng với H2SO4 loãng. - Bài toán hỗn hợp kim loại tác dụng với H2SO4 đặc. - Bài toán tổng hợp về tính chất của H2SO4. Số câu hỏi 4 7 4 1 16 Số điểm 1,2 2,1 1,6 0,4 5,3 điểm (53%) Tổng số câu 8 11 8 2 30 Tổng số điểm 2,4đ (24%) 3,6đ (36%) 3,2đ (32%) 0,8 (8%) 10,0 đ Họ, tên học sinh: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .Số báo danh: . . . . . . . . . . . ................ SỞ GD-ĐT NINH THUẬN Trường THPT Trường Chinh ********* (đề kiểm tra có 2 trang) ĐỀ KIỂM TRA HỌC KỲ II NĂM HỌC 2015-2016 MÔN: HÓA HỌC LỚP 10. Chương trình chuẩn Thời gian làm bài: 45 phút (không kể thời gian phát đề) Mã đề thi 210 Cho nguyên tử khối của các nguyên tố : H = 1; C = 12; O = 16; S=32; Li=7; Na = 23; K=39; Rb=85; Zn=65; Mg=24; Al=27; Fe=56; Cu=64; Cl=35,5; Mn=55 Câu 1: Kim loại nào sau đây sẽ bị thụ động khi gặp dung dịch H2SO4 đặc, nguội? A. Al và Fe B. Al và Zn. C. Fe và Mg. D. Fe và Cu. Câu 2: Chất nào sau đây được dùng để tẩy màu, sát trùng ? A. N2 B. CaOCl2 C. NaOH D. KNO3 Câu 3: Cho phản ứng hóa học: Cl2 + 2NaOH NaCl + NaClO + H2O. Vai trò của Cl2 trong phản ứng này là: A. Không là chất oxi hóa, không là chất khử B. Chất oxi hóa C. Chất khử D. Vừa là chất oxi hóa, vừa là chất khử Câu 4: Chất dùng để chữa sâu răng trong y học là: A. H2S B. O2 C. O3 D. Cl2 Câu 5: Chất khí màu vàng lục, rất độc là: A. SO2 B. Cl2 C. Br2 D. F2 Câu 6: Phản ứng được dùng để điều chế SO2 trong công nghiệp là: A. Cu + 2H2SO4(đ) CuSO4 + SO2 + 2H2O B. 4FeS2 + 11O2 2Fe2O3 + 8SO2 C. C + 2H2SO4(đ)CO2 + 2SO2 + 2H2O D. 2H2S + 3O2 2SO2 + 2H2O Câu 7: Nguyên tử của các nguyên tố F, Cl, Br, I đều có? A. 6 electron ở lớp ngoài cùng B. 1 electron ở lớp ngoài cùng C. 7 electron ở lớp ngoài cùng D. 5 electron ở lớp ngoài cùng Câu 8: Phản ứng hóa học nào sau đây chứng tỏ Cl2 có tính oxi hóa mạnh hơn Br2? A. Cl2 +2NaBr 2NaCl + Br2 B. Cl2 + H2OHCl + HClO C. Cl2 + 2NaI 2NaCl + I2 D. Br2 +2NaI 2NaBr + I2 Câu 9: Phản ứng giữa 2 chất nào sau đây xảy ra dễ dàng nhất? A. I2 và H2. B. F2 và H2. C. Br2 và H2 D. Cl2 và H2. Câu 10: Ở điều kiện thường, O3 oxi hóa được kim loại nào sau đây mà O2 không phản ứng được? A. Ag B. Mg C. Cu D. Fe Câu 11: Trong phản ứng hóa học nào sau đây, HCl thể hiện tính khử? A. Fe + 2HCl FeCl2 + H2 B. AgNO3 + HCl AgCl + HNO3 C. NaOH + HCl NaCl + H2O D. MnO2 + 4HCl MnCl2 + Cl2 + 2H2O Câu 12: Phản ứng hóa học nào sau đây được dùng để điều chế HCl trong phòng thí nghiệm? A. Cl2 + H2O HCl + HClO B. Cl2 + SO2 + 2H2O 2HCl + H2SO4 C. H2 + Cl2 2HCl D. NaCl(rắn) + H2SO4(đặc) NaHSO4 + HCl Câu 13: Phản ứng nào sau đây viết sai? A. Cu + 2H2SO4 CuSO4 + SO2 + 2H2O B. 2FeO + 4H2SO4 Fe2(SO4)3 + SO2 + 4H2O C. 2Fe + 3H2SO4 Fe2(SO4)3 + 3H2 D. CuO + H2SO4 CuSO4 + H2O Câu 14: Dung dịch HCl không phản ứng được với chất nào sau đây? A. Al(OH)3 B. Fe2O3 C. Ag D. AgNO3 Câu 15: Phản ứng hóa học nào sau đây chứng tỏ S là một chất oxi hóa? A. S+ H2 H2S B. S + 3F2SF6 C. S+O2SO2 D. S+2H2SO4đ3SO2 +2H2O Câu 16: Câu nào sau đây sai khi nhận xét về khí H2S? A. Là khí không màu, mùi trứng thối, nặng hơn không khí B. Tan ít trong nước C. Chất rất độc D. Làm xanh giấy quỳ tím ẩm Câu 17: Lưu huỳnh trong chất nào sau đây vừa có tính oxi hóa, vừa có tính khử? A. H2S B. H2SO4 C. Na2SO4 D. SO2 Câu 18: Axit nào sau đây có phản ứng với cacbon? A. Axit sunfuric đặc nóng B. Axit sufuhidric C. Axit clohidric D. Axit sunfuric loãng Câu 19: Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố S nằm ở: A. Chu kỳ 3, nhóm IVA B. Chu kì 3, nhóm VIA C. Chu kì 4, nhóm VIA D. Chu kì 3, nhóm VIIIA Câu 20: Sục khí H2S vào dung dịch Pb(NO3)2 thì hiện tượng quan sát được là: A. Không có hiện tượng gì B. Xuất hiện kết tủa màu trắng C. Xuất hiện kết tủa màu đen D. Xuất hiện kết tủa màu vàng Câu 21: Để phân biệt 3 dung dịch: Na2SO4, NaNO3, H2SO4, ta chọn thuốc thử? A. phenolphtalein và dung dịch HCl B. phenolphtalein và dung dịch Ba(NO3)2 C. quỳ tím và dung dịch BaCl2 D. quỳ tím và dung dịch NaOH Câu 22: Hòa tan hoàn toàn 15,9 gam một muối cacbonat của kim loại kiềm bằng dung dịch HCl dư thu được 3,36 lít khí (đktc). Kim loại đã cho là: A. Li B. Na C. K D. Rb Câu 23: Hấp thụ hết 6,72 lít khí SO2 (đktc) vào 400ml dung dịch NaOH 2M. Khối lượng muối thu được sau phản ứng là: A. 38,7g B. 100,8g C. 31,2g D. 37,8g Câu 24: Hòa tan 11,9 gam hỗn hợp gồm Al và Zn bằng dung dịch H2SO4 loãng, dư thu được 8,96 lít khí H2 (đktc). Thành phần trăm theo khối lượng của Zn trong hỗn hợp đã cho là: A. 54,62% B. 56,42% C. 45,38% D. 48,35% Câu 25: Cho 12,8 gam hỗn hợp X gồm Fe và FeO tác dụng hết với dung dịch H2SO4 loãng, thu được 2,24 lít khí H2 (đktc). Mặt khác, nếu cho hỗn hợp X tác dụng hoàn toàn với dung dịch H2SO4 đặc nóng, dư thấy có V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Giá trị của V là: A. 4,48 lít B. 2,24 lít C. 5,6 lít D. 6,72 lít Câu 26: Cho 15 gam hỗn hợp gồm Al và Cu phản ứng với lượng dư dung dịch HCl, thu được 6,72 lít khí H2(đktc) và m gam chất rắn không tan. Nếu cho lượng chất rắn không tan đó tác dụng hết với khí Clo thì thu được muối có khối lượng là: A. 22,05g B. 25,2g C. 20,25g D. 22,5g Câu 27: Cho 14,4 gam hỗn hợp gồm Mg và Cu tác dụng hết với dung dịch H2SO4 đặc, nóng. Sau phản ứng thu được 7,84 lít khí SO2 (sản phẩm khử duy nhất ở đktc) và m gam muối. Giá trị của m là: A. 43g B. 62g C. 56g D. 48g Câu 28: Để trung hòa 100 ml dung dịch Ba(OH)2 0,5M cần dùng V ml dung dịch HCl 0,2M. Giá trị của V là: A. 500 B. 400 C. 200 D. 250 Câu 29: Để oxi hóa hoàn toàn 14 gam bột Fe, cần vừa đủ V lít khí Cl2 (đktc). Giá trị của V là: A. 8,96 lít B. 6,72 lít C. 5,6 lít D. 8,4 lít Câu 30: Cho 13,05 gam MnO2 tác dụng hết với dung dịch HCl đặc, đun nóng thu được V lít khí Cl2 (đktc). Giá trị của V là: A. 2,24 B. 3,36 C. 5,6 D. 4,48 ----------------------------------------------- ----------- HẾT ---------- ĐÁP ÁN KIỂM TRA HỌC KỲ II HÓA HỌC 10 Năm học: 2015-2016 Câu Đề 134 Đề 210 Đề 356 Đề 483 Điểm 1 A A D A 0,3 2 D B A D 0,3 3 A D B A 0,3 4 C C A D 0,3 5 A B B C 0,3 6 B B C B 0,3 7 C C A B 0,3 8 C A B C 0,3 9 B B C C 0,3 10 C A D B 0,3 11 D D A A 0,3 12 B D B C 0,3 13 D C C A 0,3 14 B C D B 0,3 15 B A C B 0,3 16 A D D A 0,3 17 D D A D 0,3 18 C A B C 0,3 19 A B C D 0,3 20 D C D D 0,3 21 A C D D 0,4 22 D B C C 0,4 23 A D D B 0,4 24 A A A D 0,4 25 B A A C 0,4 26 B C B C 0,4 27 C D C A 0,4 28 A A B B 0,4 29 C D D C 0,4 30 D B B A 0,4
Tài liệu đính kèm:
 de_kiem_tra_hoc_ky_ii_lop_10_mon_hoa.doc
de_kiem_tra_hoc_ky_ii_lop_10_mon_hoa.doc





