Bài kiểm tra số 2 lớp 10 - Môn: Hóa Học
Câu 1 : Cho 1,2g một kim loại nhóm IIA tác dụng hết với dung dịch HCl dư thu được 1,12 lit khí hiđro ( ở đktc ). Kim loại đó là :
A. 39K B. 12C C. 40Ca D. 24Mg
Câu 2 : Nguyên tử của các nguyên tố trong một chu kì có cùng số:
A. Nơtron B. Electron hóa trị C. Proton D. Lớp electron
Câu 3 : Nguyên tử của nguyên tố X có số hạt mang điện dương trong hạt nhân là 15. Vị trí của X trong bảng tuần hoàn là:
A. Chu kì 3, nhóm VIIA B. Chu kì 3, nhóm VA
C. Chu kì 3, nhóm IIIA D. Chu kì 2, nhóm IIIA
Câu 4 : Nguyên tố X nằm ở ô 16 thì số electron hóa trị của X là:
A. 7 B. 5 C. 6 D. 16
Câu 5 : Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kì, có tổng số hiệu nguyên tử là 23. X và Y thuộc chu kì và các nhóm nào sau đây ?
A. Chu kì 3 và các nhóm IA và IIA. B. Chu kì 3 và các nhóm IIA và IIIA.
C. Chu kì 2 và các nhóm IIIA và IVA. D. Chu kì 2 và các nhóm IIA và IIIA.
Câu 6 : Nguyên tố R có công thức oxit cao nhất là R2O7. Vậy công thức hợp chất khí với hiđro là:
A. RH3 B. RH C. RH7 D. RH2
Câu 7 : Nguyên tố R có hóa trị cao nhất với oxi là a và hóa trị trong hợp chất với hiđro là b. Biết a – b = 0. Vậy R thuộc nhóm nào trong bảng tuần hoàn?
A. Nhóm IIA B. Nhóm IVA C. Nhóm VIIA D. Nhóm IA
Câu 8 : Tìm câu sai trong các câu sau đây:
A. Bảng tuần hoàn gồm có các ô nguyên tố, các chu kỳ và các nhóm.
B. Bảng tuần hoàn có 8 nhóm A và 8 nhóm B.
C. Bảng tuần hoàn có 7 chu kỳ. Số thứ tự của chu kỳ bằng số phân lớp electron trong nguyên tử.
D. Chu kỳ là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được sắp xếp theo chiều điện tích hạt nhân tăng dần.
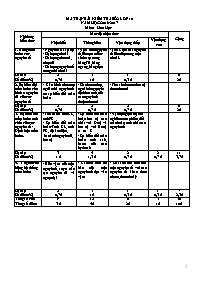
MA TRẬN BÀI KIỂM TRA SỐ 2 LỚP 10 NĂM HỌC: 2016-2017 Môn: Hóa Học Nội dung kiến thức Mức độ nhận thức Cộng Nhận biết Thông hiểu Vận dụng thấp Vận dụng cao 1. Bảng tuần hoàn các nguyên tố - Nguyên tắc sắp xếp - Số lượng chu kì - Số lượng nhóm A, nhóm B - Số lượng nguyên tố trong mỗi chu kì - Vị trí mỗi nguyên tố liên quan đến: số thứ tự trong bảng TH, hàng ngang, hàng dọc - Tìm Z của hai nguyên tố liên tiếp trong một chu kì. Số câu Số điểm(%) 2 0,7 đ 3 1 đ 1 0,3 đ 6 2đ 2. Sự biến đồi tuần hoàn cấu hình e nguyên tử của các nguyên tố - Cấu hình electron ngtử mỗi nguyên tố có sự biến đổi tuần hoàn - Số electron lớp ngoài cùng quyết định hóa tính của các nguyên tố thuộc nhóm A - Tìm số electron hóa trị theo nhóm A Số câu Số điểm(%) 2 0,7 đ 2 0,7 đ 2 0,7 đ 6 2đ 3. Sự biến đồi tuần hoàn tính chất của các nguyên tố - Định luật tuần hoàn. - Thế nào là tính KL, tính PK - Sự biến đổi tuần hoàn: Tính KL, tính PK, độ âm điện, bán kính nguyên tử, hóa trị - Sự biến đổi tuần hoàn hóa trị cao nhất với O(n) và hóa trị với H(m) n + m = 8 - Sự biến đổi tuần hoàn tính axit, bazơ của các hyđroxit - Vận dụng qui luật để nghiên cứu sự biến đổi tuần hoàn tính chất các nguyên tố Số câu Số điểm(%) 3 1 đ 4 1,3 đ 2 0,7 đ 2 0,7 đ 11 3,7đ 4. Ý nghĩa của bảng hệ thống tuần hoàn - Biết vị trí của một nguyên tố, suy ra cấu tạo nguyên tử và ngược lại - Các hóa tính cơ bản của một nguyên tố dựa vào vị trí - So sánh hóa tính của một nguyên tố với các nguyên tố khác theo nhóm, theo chu kỳ Số câu Số điểm(%) 2 0,7 đ 3 1 đ 1 0,3 đ 1 0,3 đ 7 2,3đ Tổng số câu Tổng số điểm 9 3 đ 12 4 đ 6 2đ 3 1đ 30 10đ SỞ GD-ĐT NINH THUẬN ĐỀ KIỂM TRA 1 TIẾT (BÀI SỐ 2) - LỚP 10 TRƯỜNG THPT BÁC ÁI NĂM HỌC 2016-2017 Môn: Hóa học – Chương trình chuẩn Mã đề: 117 Thời gian làm bài: 45 phút (Không kể thời gian phát đề) Đề ra: (Đề kiểm tra có 02 trang) Câu 1 : Cho 1,2g một kim loại nhóm IIA tác dụng hết với dung dịch HCl dư thu được 1,12 lit khí hiđro ( ở đktc ). Kim loại đó là : A. 39K B. 12C C. 40Ca D. 24Mg Câu 2 : Nguyên tử của các nguyên tố trong một chu kì có cùng số: A. Nơtron B. Electron hóa trị C. Proton D. Lớp electron Câu 3 : Nguyên tử của nguyên tố X có số hạt mang điện dương trong hạt nhân là 15. Vị trí của X trong bảng tuần hoàn là: A. Chu kì 3, nhóm VIIA B. Chu kì 3, nhóm VA C. Chu kì 3, nhóm IIIA D. Chu kì 2, nhóm IIIA Câu 4 : Nguyên tố X nằm ở ô 16 thì số electron hóa trị của X là: A. 7 B. 5 C. 6 D. 16 Câu 5 : Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kì, có tổng số hiệu nguyên tử là 23. X và Y thuộc chu kì và các nhóm nào sau đây ? A. Chu kì 3 và các nhóm IA và IIA. B. Chu kì 3 và các nhóm IIA và IIIA. C. Chu kì 2 và các nhóm IIIA và IVA. D. Chu kì 2 và các nhóm IIA và IIIA. Câu 6 : Nguyên tố R có công thức oxit cao nhất là R2O7. Vậy công thức hợp chất khí với hiđro là: A. RH3 B. RH C. RH7 D. RH2 Câu 7 : Nguyên tố R có hóa trị cao nhất với oxi là a và hóa trị trong hợp chất với hiđro là b. Biết a – b = 0. Vậy R thuộc nhóm nào trong bảng tuần hoàn? A. Nhóm IIA B. Nhóm IVA C. Nhóm VIIA D. Nhóm IA Câu 8 : Tìm câu sai trong các câu sau đây: A. Bảng tuần hoàn gồm có các ô nguyên tố, các chu kỳ và các nhóm. B. Bảng tuần hoàn có 8 nhóm A và 8 nhóm B. C. Bảng tuần hoàn có 7 chu kỳ. Số thứ tự của chu kỳ bằng số phân lớp electron trong nguyên tử. D. Chu kỳ là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được sắp xếp theo chiều điện tích hạt nhân tăng dần. Câu 9 : Các nguyên tố Al, Na, Mg cùng chu kì 3 có số hiệu nguyên tử lần lượt là 13, 11, 12. Thứ tự giảm dần tính kim loại là: A. Na > Al > Mg B. Al > Na > Mg C. Na > Mg > Al D. Mg > Al > Na Câu 10 : Nguyên tử của nguyên tố Y có cấu hình electron lớp ngoài cùng là 3s23p5. Vị trí của Y trong bảng tuần hoàn: A. Chu kỳ 3, nhóm VA B. Chu kỳ 3, nhóm VIIA C. Chu kỳ 5, nhóm IIIA D. Chu kỳ 4, nhóm VIA Câu 11 : Các nguyên tố thuộc cùng một nhóm A có tính chất hóa học tương tự nhau, vì vỏ nguyên tử của các nguyên tố nhóm A có: A. Số electron hóa trị như nhau B. Số electron như nhau C. Số lớp electron như nhau D. Cùng số electron s hay p Câu 12 : Nguyên tố X có số thứ tự là 18, chu kì 3, nhóm VIIIA. Điều khẳng định nào sau đây về X là sai ? A. Nguyên tố X thuộc nhóm kim loại kiềm. B. Số e ở vỏ nguyên tử là 18. C. Cấu hình e lớp ngoài cùng của X là: 3s2 3p6 D. Vỏ của nguyên tử X có 3 lớp e và 8 e hóa trị. Câu 13 : Cho các nguyên tố A, B, C, D, E lần lượt có cấu hình e như sau: (A) 1s2 2s2 2p6 3s2 (B) 1s2 2s2 2p6 3s2 3p6 4s1 (C) 1s2 2s2 2p6 3s2 3p6 4s2 (D) 1s2 2s2 2p6 3s2 3p2 (E) 1s2 2s2 2p6 3s2 3p1. Các nguyên tố thuộc cùng nhóm A là: A. A, C B. B, E C. A, C, D D. A, D, E Câu 14 : Nguyên tố M ở chu kì 3, nhóm IA. Nguyên tố G ở chu kì 2, nhóm VIA. Vậy tổng số hiệu ngtử của M và G là: A. 8 B. 11 C. 19 D. 18 Câu 15 : Nguyên tố M thuộc nhóm IVA. Trong oxit cao nhất, nguyên tố M chiếm 27,3% về khối lượng. Khối lượng nguyên tử của M là: A. 24 đvC B. 12 đvC C. 32 đvC D. 28 đvC Câu 16 : Chỉ ra nội dung đúng : “ Trong 1 chu kì, theo chiều tăng dần điện tích hạt nhân thì” A. Tính phi kim giảm dần B. Hóa trị với Oxi giảm dần C. Độ âm điện giảm dần D. Tính kim loại giảm dần Câu 17 : Các nguyên tố được sắp xếp trong bảng tuần hoàn không tuân theo nguyên tắc nào sau đây? A. Các nguyên tố được sắp xếp theo chiều tăng dần khối lượng nguyên tử. B. Các nguyên tố được sắp xếp theo chiều tăng dần của điện tích hạt nhân. C. Các nguyên tố có cùng số electron hoá trị được xếp vào một cột. D. Các nguyên tố có cùng số lớp electron được xếp vào một hàng. Câu 18 : Các nguyên tố xếp ở chu kì 6 có số lớp electron trong nguyên tử là A. 3 B. 6 C. 4 D. 5 Câu 19 : Nguyên tố hoá học nào sau đây có tính chất hoá học tương tự nguyên tố K(Z=19)? A. Na (Z=11) B. Ca (Z=20) C. Mg (Z=12) D. Al (Z=13) Câu 20 : Nguyên tố M thuộc chu kì 3 nhóm IIIA.Tính chất của nguyên tố M là: A. Kim loại hoặc phi kim B. Phi kim C. Kim loại D. Khí hiếm Câu 21 : Nguyên tố nào trong số các nguyên tố sau đây có công thức oxit cao nhất là R2O5? A. 12Mg B. 14Si C. 15P D. 13Al Câu 22 : Nguyên tố R có cấu hình electron: 1s22s22p63s23p3. Công thức oxit cao nhất và công thức hợp chất với hiđro là: A. R2O3, RH3 B. R2O5, RH5 C. R2O3, RH5 D. R2O5, RH3 Câu 23 : M là nguyên tố nhóm IIIA, oxit của nó có công thức là: A. MO3 B. M2O3 C. MO D. M2O Câu 24 : Nguyên tố X có cấu hình electron nguyên tử là 1s2 2s2 2p6 3s2 3p6 4s2. Cấu hình của ion X2+ là: A. 1s22s22p63s2 B. 1s22s22p63s23p6 4s2 C. 1s22s22p63s23p5 D. 1s22s22p63s23p6 Câu 25 : Một nguyên tố X có tổng số các hạt trong nguyên tử bằng 34. Biết nguyên tố đó thuộc nhóm IA. Nguyên tử khối của X: A. 24 B. 11 C. 23 D. 10 Câu 26 : Cấu hình e nguyên tử của nguyên tố A thuộc chu kỳ 4, nhóm IIA là: A. 1s2 2s2 2p6 3s2 3p6 4s2 B. 1s2 2s2 2p6 3s2 3p6 3d10 4s2 C. 1s2 2s2 2p4 D. 1s22s22p63s23p2 Câu 27 : Nhóm VIIIA trong bảng tuần hoàn có tên gọi: A. Nhóm khí hiếm B. Nhóm halogen C. Nhóm kim loại kiềm D. Nhóm kim loại kiềm thổ Câu 28 : Nguyên tử của các nguyên tố có cấu hình electron ở lớp ngoài cùng lần lượt như sau: X: 3s1 ; Y: 3s23p5 ; M: 3s23p6 ; N: 3s23p1 Mệnh đề nào sau đây sai ? A. Nguyên tố X, N là kim loại; Y là phi kim; M là khí hiếm . B. Cả 4 nguyên tố đều thuộc chu kì 3. C. Có một nguyên tố là khí hiếm. D. Các nguyên tố X, Y là kim loại; M, N là phi kim. Câu 29 : Cho dãy các nguyên tố nhóm IA theo thứ tự ĐTHN tăng dần là: Li – Na – K – Rb. Tính kim loại thay đổi như thế nào? A. Không đổi B. Tăng dần C. Tăng rồi giảm D. Giảm dần Câu 30 : Số chu kì lớn và chu kì nhỏ trong bảng tuần hoàn là: A. 3 và 5 B. 2 và 5 C. 3 và 4 D. 4 và 3 --- Hết --- SỞ GD – ĐT NINH THUẬN TRƯỜNG THPT BÁC ÁI Đề chính thức ĐỀ KIỂM TRA 1 TIẾT (BÀI SỐ 2) – LỚP 10 NĂM HỌC 2016 – 2017 Môn: Hóa học – Chương trình chuẩn BẢNG ĐÁP ÁN ĐỀ 117 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 D D B C A B B C C B A A A C B 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 D A B A C C D B D C A A D B D
Tài liệu đính kèm:
 bai_kiem_tra_so_2_lop_10_mon_hoa_hoc.doc
bai_kiem_tra_so_2_lop_10_mon_hoa_hoc.doc





