Bài kiểm tra số 1 lớp 10 - Môn: Hóa Học
Câu 1 : Trong nguyên tử có tổng số hạt p và n là:
A. 25 B. 80 C. 55 D. 30
Câu 2 : Cho các kí hiệu nguyên tử : ; ; ; ; ; ; . Cặp nguyên tử nào là đồng vị của cùng một nguyên tố?
A. X và M; E và R B. X và Y; Z và T C. X và T; M và E D. X và Z; Y và M
Câu 3 : Ở trạng thái cơ bản, nguyên tử của nguyên tố X có 5e ở lớp L. Số proton của nguyên tử X là:
A. 5 B. 6 C. 8 D. 7
Câu 4 : Trong nguyên tử, hạt mang điện là:
A. Proton, electron B. Proton, nơtron C. Electron D. Electron, nơtron
Câu 5 : Trong tự nhiên, Clo có 2 đồng vị, trong đó đồng vị 35Cl chiếm 75,77%, còn lại là đồng vị thứ 2. Biết rằng = 35,5. Số khối của đồng vị thứ 2 là: (coi số khối chính là nguyên tử khối)
A. 36 B. 34 C. 38 D. 37
Câu 6 : Biết rằng Z là đại lượng đặc trưng cho nguyên tử của một nguyên tố hóa học. Vậy khẳng định nào sau đây là thiếu chính xác?
A. Số khối = Z B. Số proton = Z C. Số electron = Z D. Số hiệu nguyên tử = Z
Câu 7 : “Trên vỏ nguyên tử, các electron chuyển động xung quanh hạt nhân.”. Hãy chọn cụm từ thích hợp đối với chỗ trống ở trên.
A. Với vận tốc rất lớn không theo quỹ đạo xác định B. Với vận tốc rất lớn có quỹ đạo hình elip hay hình tròn
C. Một cách tự do D. Với vận tốc rất lớn trên những quỹ đạo xác định
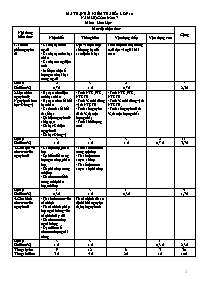
MA TRẬN BÀI KIỂM TRA SỐ 1 LỚP 10
NĂM HỌC: 2016-2017
Môn: Hóa Học
Nội dung
kiến thức
Mức độ nhận thức
Cộng
Nhận biết
Thông hiểu
Vận dụng thấp
Vận dụng cao
1. Thành phần nguyên tử
- Các hạt tạo nên ng.tử
- Các hạt tạo nên hạt nhân
- Các hạt mang điện tích
- Mối quan hệ số lượng các loại hạt trong ng.tử
Dựa vào quan hệ số lượng hạt để xác định số hạt
Tính được các hạt trong n.tử dựa vào giải bài toán
Số câu
Số điểm(%)
2
0,7 đ
3
1 đ
2
0,7đ
7
2,3đ
2. Hạt nhân nguyên tử-Nguyên tố hoá học-Đồng vị
- Hạt tạo nên điện tích hạt nhân
- Hạt tạo nên số khối hạt nhân
- Cách tính số khối từ số hạt
- Số hiệu nguyên tử-số hạt p,e
- Số hạt-Kí hiệu nguyên tử
- Số hạt-Đồng vị
- Tính NTK, PTK, NTKTB
- Tính % mỗi đồng vị từ NTKTB
- Tính số nguyên tử từ %,từ một lượng chất
- Tính khối lượng mol
- Tính NTK, PTK, NTKTB
- Tính % mỗi đồng vị từ NTKTB
- Tính số nguyên tử từ %,từ một lượng chất
Số câu
Số điểm(%)
3
1 đ
3
1 đ
3
1 đ
2
0,7 đ
11
3,7đ
3. Cấu tạo vỏ electron của nguyên tử
- Kí hiệu lớp,phân lớp
- Sự biến đổi năng lượng các lớp,phân lớp
- Số phân lớp trong mỗi lớp
- Số electron tối đa trong mỗi phân lớp,mỗi lớp
- Tính số electron trong một lớp
- Từ số electron suy ra số lớp
- Từ số electron suy ra số phân lớp
Số câu
Số điểm(%)
1
0,3 đ
3
1 đ
1
0,3 đ
5
1,7đ
4. Cấu hình electron của nguyên tử
- Từ số electron viết cấu hình
- Từ cấu hình phân lớp ngoài cùng viết cấu hình đầy đủ
- Số electron lớp ngoài cùng
- Đặc điểm số electron lớp ngoài cùng
Từ cấu hình đi xác định khối nguyên tố,loại nguyên tố
Số câu
Số điểm(%)
3
1 đ
3
1 đ
1
0,3 đ
7
2,3đ
Tổng số câu
Tổng số điểm
9
3 đ
12
4 đ
6
2đ
3
1đ
30
10đ
SỞ GD-ĐT NINH THUẬN ĐỀ KIỂM TRA 1 TIẾT (BÀI SỐ 1) LỚP 10
TRƯỜNG THPT BÁC ÁI NĂM HỌC 2016-2017
Môn: Hóa học – Chương trình chuẩn
Thời gian làm bài: 45 phút
Mã đề: 105
(Không kể thời gian phát đề)
Đề ra: (Đề kiểm tra có 02 trang)
Câu 1 :
Trong nguyên tử có tổng số hạt p và n là:
A.
25
B.
80
C.
55
D.
30
Câu 2 :
Cho các kí hiệu nguyên tử : ; ; ; ; ; ; . Cặp nguyên tử nào là đồng vị của cùng một nguyên tố?
A.
X và M; E và R
B.
X và Y; Z và T
C.
X và T; M và E
D.
X và Z; Y và M
Câu 3 :
Ở trạng thái cơ bản, nguyên tử của nguyên tố X có 5e ở lớp L. Số proton của nguyên tử X là:
A.
5
B.
6
C.
8
D.
7
Câu 4 :
Trong nguyên tử, hạt mang điện là:
A.
Proton, electron
B.
Proton, nơtron
C.
Electron
D.
Electron, nơtron
Câu 5 :
Trong tự nhiên, Clo có 2 đồng vị, trong đó đồng vị 35Cl chiếm 75,77%, còn lại là đồng vị thứ 2. Biết rằng = 35,5. Số khối của đồng vị thứ 2 là: (coi số khối chính là nguyên tử khối)
A.
36
B.
34
C.
38
D.
37
Câu 6 :
Biết rằng Z là đại lượng đặc trưng cho nguyên tử của một nguyên tố hóa học. Vậy khẳng định nào sau đây là thiếu chính xác?
A.
Số khối = Z
B.
Số proton = Z
C.
Số electron = Z
D.
Số hiệu nguyên tử = Z
Câu 7 :
“Trên vỏ nguyên tử, các electron chuyển động xung quanh hạt nhân................”. Hãy chọn cụm từ thích hợp đối với chỗ trống ở trên.
A.
Với vận tốc rất lớn không theo quỹ đạo xác định
B.
Với vận tốc rất lớn có quỹ đạo hình elip hay hình tròn
C.
Một cách tự do
D.
Với vận tốc rất lớn trên những quỹ đạo xác định
Câu 8 :
Cấu hình electron nào dưới đây không đúng:
A.
1s22s22p63s1
B.
1s22s22p63s23p44s2
C.
1s22s22p63s23p3
D.
1s22s22p63s23p63d54s2
Câu 9 :
Sự phân bố electron vào các lớp và phân lớp căn cứ vào:
A.
Mức năng lượng tăng dần
B.
Số khối tăng dần
C.
Điện tích hạt nhân tăng dần
D.
Số electron tăng dần
Câu 10 :
Nguyên tử nguyên tố X có phân lớp electron ngoài cùng là 3d5. Số electron trong lớp vỏ nguyên tử X là:
A.
24
B.
20 hoặc 21
C.
25
D.
24 hoặc 25
Câu 11 :
Cấu hình electron của nguyên tử X là 1s² 2s²2p6 3s². Biết rằng X có số khối là 24 thì trong hạt nhân của X có:
A.
12 nơtron
B.
11 nơtron
C.
24 proton
D.
13 nơtron
Câu 12 :
Cấu hình electron nào sau đây là của phi kim?
A.
1s² 2s² 2p6 3s² 3p6
B.
1s² 2s² 2p6 3s² 3p1
C.
1s² 2s²2p6 3s²
D.
1s² 2s² 2p6 3s² 3p3
Câu 13 :
Số lớp electron của nguyên tử: ; lần lượt là?
A.
3 và 4
B.
7 và 12
C.
1 và 3
D.
2 và 3
Câu 14 :
Cho biết số hiệu nguyên tử của đồng là Z = 29 và lớp ngoài cùng có 1 electron. Vậy cấu hình electron đúng của Cu là:
A.
[Ar]4s24p25s1
B.
[Ar]4s24p1
C.
[Ar]3d104s1
D.
[Ar]3d84s1
Câu 15 :
Số đơn vị điện tích hạt nhân của nguyên tử flo là 9. Số electron ở phân mức năng lượng cao nhất là:
A.
7
B.
2
C.
5
D.
9
Câu 16 :
Trong nguyên tử, các electron quyết định tính chất của kim loại, phi kim hay khí hiếm là:
A.
Các electron lớp M
B.
Các electron lớp ngoài cùng
C.
Các electron lớp L
D.
Các electron lớp K
Câu 17 :
Electron thuộc lớp nào sau đây liên kết với hạt nhân chặt chẽ nhất?
A.
Lớp N
B.
Lớp K
C.
Lớp L
D.
Lớp M
Câu 18 :
Cấu hình electron của nguyên tử biểu diễn:
A.
Sự phân bố electron trên các phân lớp thuộc các lớp khác nhau
B.
Sự chuyển động của electron trong nguyên tử.
C.
Thứ tự các lớp và phân lớp electron.
D.
Thứ tự các mức và phân mức năng lượng.
Câu 19 :
Nguyên tử A có tổng số hạt cơ bản là 40. Biết nguyên tử A có tổng số e trên các phân lớp p là 7. Số hiệu nguyên tử A là:
A.
12
B.
7
C.
11
D.
13
Câu 20 :
Lớp ngoài cùng có số e tối đa là:
A.
7
B.
8
C.
5
D.
4
Câu 21 :
Nguyên tử canxi có kí hiệu là . Phát biểu nào sau đây sai?
A.
Số hiệu nguyên tử của Ca là 20.
B.
Tổng số hạt trong nguyên tử Ca là 40.
C.
Nguyên tử Ca có 2 electron lớp ngoài cùng.
D.
Trong nguyên tử Ca, lớp electron có mức năng lượng cao nhất là lớp N.
Câu 22 :
Dựa vào thứ tự mức năng lượng, xét xem sự sắp xếp các phân lớp nào sau đây sai:
A.
3d < 4s
B.
4s > 3s
C.
3p < 3d
D.
1s < 2s
Câu 23 :
Một nguyên tử X có tổng số hạt p, n, e bằng 30. Trong nguyên tử X có số hạt mang điện dương bằng số hạt không mang điện. Số khối của nguyên tử X là:
A.
30
B.
40
C.
20
D.
10
Câu 24 :
Cấu hình electron nào sau đây là của nguyên tử Fe (Z=26)?
A.
[Ar] 3d74s1
B.
[Ar] 3d54s3
C.
[Ar] 3d64s2
D.
[Ar] 3d8
Câu 25 :
Cho cấu hình electron của nguyên tử R: 1s22s22p63s23p6 . R là nguyên tố:
A.
Phi kim
B.
Khí hiếm
C.
Kim loại
D.
Không xác định được
Câu 26 :
Nguyên tử M có 11 electron và có số nơtron nhiều hơn số proton 1 hạt. Kí hiệu nguyên tử của M:
A.
M
B.
M
C.
M
D.
M
Câu 27 :
Cho các nguyên tố có số hiệu nguyên tử lần lượt là X(Z=1); Y (Z=3); M(Z=7); T(Z=18); R(Z=19). Dãy gồm các nguyên tố kim loại là?
A.
X, Y, R
B.
M, T
C.
X, R
D.
Y, R
Câu 28 :
Nguyên tố Agon có 3 đồng vị: (99,6%) ; (0,34%) ; (0,06%). Nguyên tử khối trung bình của Agon có giá trị là:
A.
39,75
B.
39,99
C.
38,25
D.
37,55
Câu 29 :
Nguyên tử của nguyên tố nào sau đây có số electron lớp ngoài cùng lớn nhất?
A.
Mg (Z=12)
B.
K (Z=20)
C.
F (Z=9)
D.
C (Z=6)
Câu 30 :
Nguyên tử X có tổng số hạt p, n, e là 48 và số khối là 32. Cấu hình e của X là:
A.
1s2 2s2 2p6 3s2 3p6
B.
1s2 2s2 2p6 3s2 3p4
C.
1s2 2s2 2p6 3s2 3p5
D.
1s2 2s2 2p6 3s2 3p6 3d104s2 4p2
--- Hết ---
SỞ GD – ĐT NINH THUẬN
TRƯỜNG THPT BÁC ÁI
Đề chính thức
ĐỀ KIỂM TRA 1 TIẾT (BÀI SỐ 1) – LỚP 10
NĂM HỌC 2016 – 2017
Môn: Hóa học – Chương trình chuẩn
Thời gian làm bài: 45 phút
(Không kể thời gian phát đề)
BẢNG ĐÁP ÁN ĐỀ 105
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
C
D
D
A
D
A
A
B
A
C
A
D
D
C
C
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
B
B
A
D
B
B
A
C
C
B
A
D
B
C
B
phiÕu soi - ®¸p ¸n (Dµnh cho gi¸m kh¶o)
M«n : Hoa 10 -1
M· ®Ò : 105
01
{ | ) ~
28
{ ) } ~
02
{ | } )
29
{ | ) ~
03
{ | } )
30
{ ) } ~
04
) | } ~
05
{ | } )
06
) | } ~
07
) | } ~
08
{ ) } ~
09
) | } ~
10
{ | ) ~
11
) | } ~
12
{ | } )
13
{ | } )
14
{ | ) ~
15
{ | ) ~
16
{ ) } ~
17
{ ) } ~
18
) | } ~
19
{ | } )
20
{ ) } ~
21
{ ) } ~
22
) | } ~
23
{ | ) ~
24
{ | ) ~
25
{ ) } ~
26
) | } ~
27
{ | } )
Tài liệu đính kèm:
 bai_kiem_tra_so_1_lop_10_mon_hoa_hoc.doc
bai_kiem_tra_so_1_lop_10_mon_hoa_hoc.doc





